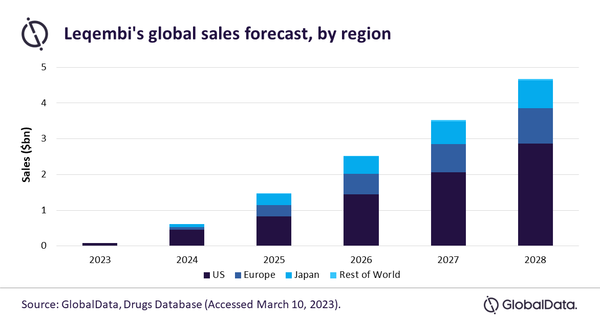
바이오젠/에자이 ‘레켐비’ 2028년까지 129억$ 매출 예상
경쟁자 릴리 ‘도나네맙’ 승인 거부로 수년간 톱셀링 유지
새로운 알츠하이머 치료제는 황금알을 낳는 거위가 될 수 있을 전망이다.
바이오젠/에자이의 레켐비(Leqembi, lecanemab)는 지난 1월 알츠하이머병 치료에 미국 FDA에서 승인을 받았다.
이 약품은 현재 유럽과 일본 등에서 승인 심사 중에 있다.
이런 지역들에서 승인이 되면, 레켐비는 앞으로 몇 년 동안 알츠하이머병에 대해 톱셀링 약품으로 입지를 굳힐 수 있다.
데이터 및 분석 회사인 글로벌데이터에 따르면, 레켐비는 2023~2028년 사이에 총 예상 매출 129억 달러로, 블록버스터가 될 것으로 예상된다.
2023년과 2028년 사이에 총 매출 7억 6200만 달러로 예상되는 두 번째 최대 승인된 알츠하이머 치료제인 아리셉트(Aricept)보다, 레켐비의 예상 매출이 17배 능가할 것으로 추정된다.
레켐비의 최대 시장은 2023-28년 예상 매출 중 77억 달러에 이를, 미국이 될 것으로 예상된다.
미국 시장은 2028년까지 연평균 약 106%의 고성장해 레켐비 전체 매출의 60%를 차지할 것으로 예상됨에 따라 약품의 상업적 성공을 견인하는 핵심 역할을 하고 있다.
올해 10월 유럽과 일본에서 레켐비의 예상된 승인은 매출을 더 확대할 것으로 기대된다.
이런 지역의 매출은 2023-28년 총 매출 점유율의 39%를 차지해, 2028년까지 연평균 77% 폭발적 성장이 예상된다.
레켐비는 아밀로이드 베타 A4 단백질을 표적으로 하고 알츠하이머병 치료에 임상적으로 중요한 것으로 생각되는 아밀로이드 베타 플라크를 선택적으로 결합하고 제거함으로써 작용하는 단클론항체이다.
레켐비의 FDA 승인은 2상 Athena AD 임상시험의 데이터를 근거로 했다.
연구결과, 레켐비 치료는 뇌에서 아밀로이드 베타 플라크의 양을 크게 감소시켰고 위약군에 비해 레켐비 치료 환자에서 통계적으로 유의한 인지 감소를 보였다.
바이오젠과 에자이는 레켐비가 장기적인 건강 결과에 긍정적인 영향을 미칠 수 있다는 연구결과를 Neurology and Therapy 저널 최신호에 게재했다.
분석은 레켐비의 효능과 안전성을 평가한 3상 Clarity AD 임상시험 데이터와 질병의 자연스러운 진행을 시뮬레이션하기 위해 발표된 문헌을 사용한 질병 시뮬레이션 모델을 기반으로 했다.
시뮬레이션에서 표준요법 단독 환자와 비교해, 레켐비+표준요법을 받은 환자는 경도, 중등도, 중증 알츠하이머AD 치매로 질병 진행의 추정된 평생 위험이 각각 7.5%, 13.7%, 8.8% 감소했다.
또한, 레켐비 그룹은 표준요법 단독 그룹에 비해 0.71 품질 보정 수명(QALYs)의 증가를 보였다.
레켐비로 치료는 알츠하이머병 진행을 지연시키고, 더 오래 살 수 있고, 삶의 질을 향상시킴으로써 현재의 표준요법보다 더 많은 이점을 제공할 수 있다고 회사 측이 밝혔다.
레켐비는 2028년까지 총 81억 달러의 매출이 예상되는 아밀로이드 베타 플라크를 표적으로 하는 유사한 단클론 항체인 릴리의 도나네맙(donanemab)과 경쟁에 직면해 있다.
하지만, 지난 1월, FDA는 도나네맙의 가속 승인에 대한 릴리의 신청을 거부했다.
레켐비는 이 공간에서 당분간 경쟁이 없게 됐다.
가속 승인에 대한 도나네맙의 신청 거부에 따라, 레켐비는 향후 몇 년 동안 알츠하이머 병에 대한 베스트셀링 약품 중 하나로 부상할 것으로 예상되는 유리한 위치에 있다고 글로벌데이터가 밝혔다.